TD Géométrie des molécules
I - Géométrie tetraédrique
1) Représentation de deux isomères envisageables pour le dibromométhane :

2) Les deux savants ont réfutés cette hyptohèse car il n'existe qu'un seul type de dibromométhane. Or on sait par 1) que en géométrie plane, on observe deux isomères.
→ Géométrie plane impossible
3) Représentation de la molécule de Bromométhane :

Il n'existe qu'un seul isomère possible, et il n'est pas précisé qu'il n'existe qu'un seul type de Bromométhane.
→ L'hypothèse d'une géométrie plane est envisageable les scientifiques ne peuvent pas tirer les mêmes conclusions
II - Molécules en trois dimensions
- Méthane CH4 : Tétraédrique
- Ammoniac NH3 : Pyramidale
- Eau H2O : Coudée
- Dioxyde de carbone CO2 : Linéaire
- Méthanal CH2O : Triangulaire
2) a)
- Géométrie de la molécule d'eau : Coudée
- Géométrie de la molécule de dioxyde de carbone : Linéaire
Les deux molécules ont même nombre d'atomes mais leur géométrie est différente
- Géométrie de la molécule d'Ammoniac : Pyramidale
- Géométrie de la molécule de Méthanal : Triangulaire
Les deux molécules ont même nombre d'atomes mais leur géométrie est différente
→ Le nombre d'atome ne permet pas de définir la géométrie des molécules
b)
- Molécule d'eau :

- Molécule de dioxyde de carbone :
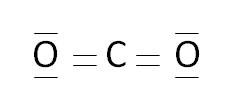
- Molécule d'Ammoniac :

- Molécule de Méthanal :

3) La représentation de Lewis ne permet pas de définir la géométrie d'une molécule. On ne peut pas distinguer les géometries linéaires des coudées. Ni les pyramidales des triangulaires.
4) a) Les doublets liants ou non liants, dit simples, sont formés d'électrons qui sont eux chargés négativement. La charge des doublets est alors négative.
b) Les doublets vont alors se repousser au maximum
c) La distance entre les atomes liés à l'atome central est la même
d) Autour d'un atome central donné,
- 4 doublets simples se répartissent en géométrie tétraédrique
- 2 liaisons simples et une liaison double se répartissent en géométrie triangulaire